La particella alla base della tecnologia moderna
Poco più di un secolo fa gli elettroni erano ancora sconosciuti. Oggi si parla di elettroni come di oggetti familiari, che con il loro moto e le loro proprietà dominano il campo dell’elettronica e dell’informatica. In tempi recenti i sistemi elettronici, sempre più miniaturizzati, sono divenuti capaci di svolgere, in dispositivi a semiconduttore più piccoli di una pulce – i cosiddetti chip – le funzioni di calcolo e di memoria che mezzo secolo fa richiedevano macchine grandi come una stanza. Sono giunti in scena dispositivi mirabolanti, nemmeno sospettabili ai tempi in cui io ero uno studente di fisica che svolgeva la tesi di laurea proprio sui materiali semiconduttori. Basta pensare al telefonino intelligente, con cui si fanno foto e video, si leggono le e-mail e i giornali, si ascolta musica, si naviga in Rete, si trasmettono immagini nello spazio lontano.
L’elettrone
Protagonista di questa rivoluzione, che sempre più regola la vita dell’uomo odierno, è una minuscola entità, un po’ particella, un po’ onda, che pesa 9,11 × 10–28 grammi e ha carica negativa pari a –1,6 × 10–19 C (dove C è l’unità di misura della carica elettrica, dal nome del celebre fisico Coulomb). Gli elettroni si trovano all’interno degli atomi, formati da un nucleo centrale carico positivamente e da un dato numero di elettroni che, in un semplice modello classico, gli orbitano attorno come pianeti: la carica totale degli elettroni è sempre eguale a quella del nucleo, cosicché l’atomo è complessivamente neutro.
Vi sono materiali, quali i metalli e i semiconduttori, nei quali parte degli elettroni non si trova legata ai rispettivi nuclei, ma può spostarsi liberamente all’interno del solido. In tal caso, quando ai capi del materiale viene applicata una differenza di potenziale elettrico, si ha passaggio di corrente. Nei semiconduttori hanno luogo anche effetti più complessi, come la rettificazione della corrente nei diodi e nei transistor a giunzione, e soprattutto nei dispositivi del genere MOS (metallo-ossido-semiconduttore), componenti base dei microprocessori.
La corrente elettrica
Nei primi tempi dopo la sua scoperta, l’elettricità per lo più era intesa come un fluido continuo. Le prime indicazioni sulla sua natura atomica si ebbero solo oltre la metà dell’Ottocento, allorché Michael Faraday studiò la scomposizione, ad opera della corrente elettrica, di un sale di metallo disciolto nell’acqua. Stabilì che la quantità del metallo che si deposita al catodo (polo negativo) è proporzionale alla quantità di carica elettrica che è fluita attraverso la soluzione: nel processo di argentatura, ad esempio, 1,118 mg di argento per ogni Coulomb transitato. Lo scienziato tedesco Hermann von Helmholtz nel 1881 suggerì che ciò era spiegabile solo se la sostanza veniva depositata atomo per atomo: ogni atomo metallico, che in soluzione si presenta ionizzato, ossia elettricamente carico, si sarebbe depositato al catodo tornando alla forma neutra grazie allo scambio con l’elettrodo di una quantità di carica, sempre multiplo intero di una carica elementare.
Non molti scienziati si trovarono d’accordo con questa visione. Occorreva un’esperienza risolutoria per fugare ogni dubbio. A cimentarsi, nel 1897, nell’esperimento fu J.J. Thomson, poi premio Nobel come scopritore dell’elettrone.
L’esperimento di J.J. Thomson
L’esperimento fu realizzato con un tubo catodico evacuato in vetro, non troppo dissimile da quelli che si impiegano nei vecchi televisori, dove un pennello collimato di elettroni, emesso da un filamento incandescente, andava a colpire la parete opposta, creando un punto luminoso. Il pennello, chiamato per l’appunto raggio catodico, passava in una zona di campo elettrico creato da due placche metalliche tra le quali veniva applicata una tensione. Il campo faceva deflettere il raggio e spostava il punto luminoso.
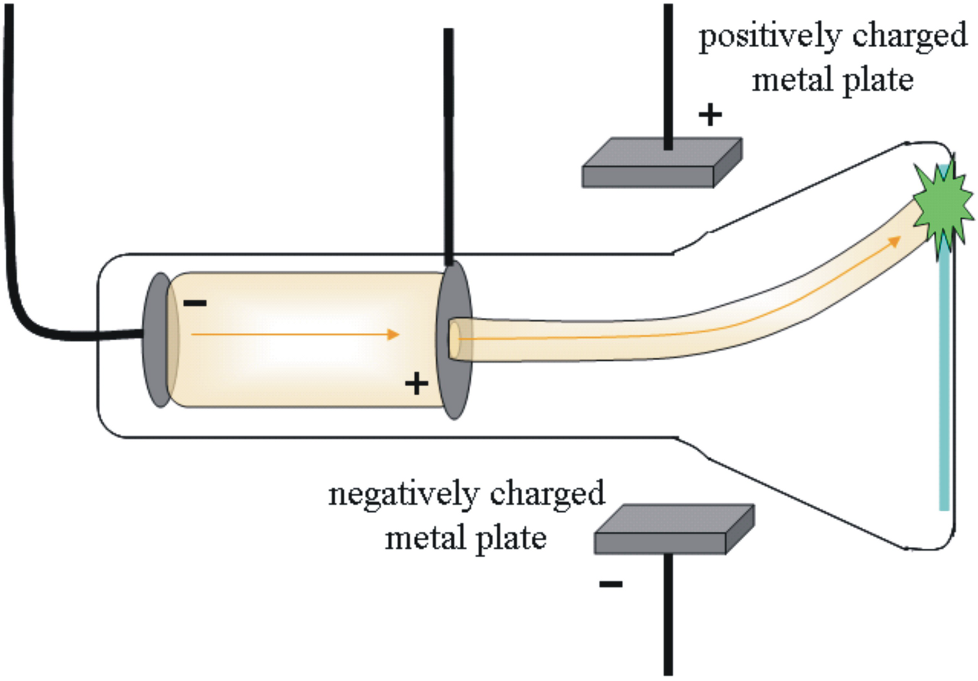
I raggi catodici non sono stati inventati da Thomson, giacché diversi altri fisici prima di lui li avevano prodotti e studiati nell’ambito più vasto dei tubi a scarica. Tuttavia, furono di Thomson due idee importanti:
- le dimensioni delle eventuali particelle devono essere molto più piccole di quelle degli atomi, in considerazione del fatto che i raggi catodici penetrano assai più facilmente all’interno dei materiali rispetto, ad esempio, ai fasci di molecole;
- in un tubo a scarica, le particelle che portano la corrente elettrica sono sempre le stesse, quale che sia il gas contenuto nel tubo. I portatori di carica, cioè, sarebbero stati dei corpuscoli universali, costituenti base della materia.
Thomson notò che lo spostamento della macchia luminosa osservato all’applicazione del campo elettrico era proporzionale alla tensione applicata tra le placche deflettrici e che avveniva nel senso previsto per un raggio costituito da “proiettili” carichi negativamente.
Il rapporto carica/massa
Ma il punto cruciale dell’esperimento fu la misura del rapporto e/m tra carica e massa della particella, un rapporto che si conosceva già per altre particelle materiali più grosse, come atomi ionizzati, e che si sarebbe potuto determinare solo nel caso si avesse a che fare effettivamente con singole particelle. L’idea di Thomson fu di sottoporre il fascio anche a un campo magnetico, orientato in direzione trasversale sia al fascio sia al campo elettrico, quindi normale rispetto al piano della figura. Ora, anche un campo magnetico fa deflettere le cariche se queste sono in moto, però l’angolo di deviazione non dipende soltanto dal valore della carica – come nel caso del campo elettrico – ma pure da quello della massa (la traiettoria subisce il cosiddetto incurvamento ciclotronico, che aumenta al crescere della massa).
Se si fa variare il campo magnetico fino a che si produce una deflessione eguale e contraria al caso elettrico, si può mostrare – chiedo fiducia ai lettori – che vale la formula e/m = Fq/B2L, dove F è la forza esercitata dal campo elettrico sulla particella, q l’angolo di deflessione (eguale nei due casi), B il campo magnetico e L la lunghezza della zona dove agiscono i campi.
Poiché tutti i parametri al secondo membro sono misurabili, Thomson poté determinare un valore di e/m oltre 1000 volte più grande che per il protone (precisamente 1836). Ma poiché gli esperimenti sull’elettrolisi suggerivano che il protone e l’elettrone avessero cariche eguali, benché di segno opposto, la conclusione fu che l’elettrone era 1836 volte più leggero del protone.
Thomson ebbe il Nobel nel 1906, l’anno successivo a quello ricevuto da Einstein per la spiegazione dell’effetto fotoelettronico.
L’architettura dell’atomo
È dalle osservazioni di Thomson che furono avviati i tentativi di definire l’architettura dell’atomo. Thomson suggerì una specie di minuscola pallina dove elettroni e protoni si trovavano mescolati. Più verosimile fu il modello proposto poco dopo dal neozelandese Ernest Rutherford, simile piuttosto a un sistema planetario dove gli elettroni ruotano attorno a un nucleo formato dai protoni raggruppati. Nel Novecento la meccanica quantistica ci ha dato la formulazione moderna dell’atomo, dove gli elettroni non sono palline, ma nuvole di carica distribuita, che sotto taluni aspetti si comportano come onde: se è vero che un raggio di elettroni può erodere del materiale proprio come ci si attenderebbe da un bombardamento di proiettili, è anche vero che esso permette di costruire microscopi elettronici, agendo proprio come un fascio di luce.
Colui che scelse il nome elettrone per la nuova particella dal grande futuro fu George Johnstone Stoney con una lettera diretta al Philosophical Magazine, pubblicata nel 1894, Vol. 38, p. 418.
Immagine di copertina: Science Museum London – Wikimedia
Immagine nel testo: credit Sharon Bewick – Wikimedia

























